CAPA Là Gì? — Corrective And Preventive Action
CAPA (Corrective And Preventive Action) là hệ thống quản lý chất lượng bắt buộc trong GMP và ICH Q10 (Pharmaceutical Quality System). CAPA bao gồm hai thành phần chính:
- Corrective Action (CA — Hành động khắc phục): Hành động loại bỏ nguyên nhân gốc của sự cố đã xảy ra để ngăn tái diễn
- Preventive Action (PA — Hành động phòng ngừa): Hành động ngăn chặn sự cố tiềm ẩn trước khi xảy ra, dựa trên phân tích trend và risk assessment
CAPA áp dụng cho mọi sai lệch trong nhà máy dược phẩm: từ HVAC, hệ thống nước, vi sinh đến quy trình sản xuất và kiểm nghiệm. CAPA là yếu tố thanh tra viên EU GMP và FDA đặc biệt quan tâm khi audit.
💡 Lưu ý chuyên gia: CAPA không phải là "điền form cho xong". Một hệ thống CAPA hiệu quả phải giảm được tỷ lệ deviation tái diễn theo thời gian. FDA đánh giá hiệu quả CAPA thông qua trending data — nếu cùng loại deviation tái diễn, CAPA được coi là ineffective.
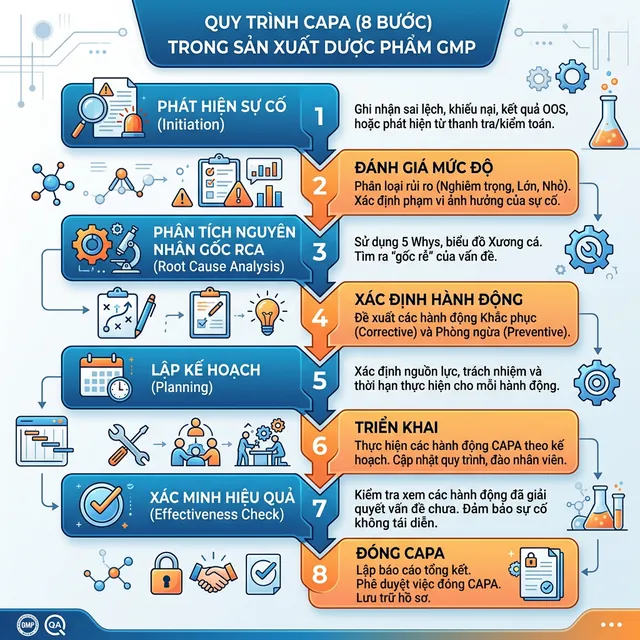
Quy Trình 8 Bước CAPA Chi Tiết
Bước 1: Phát Hiện & Ghi Nhận Sự Cố
Nguồn mở CAPA bao gồm: deviation report, OOS/OOT (Out of Specification/Trend), khiếu nại khách hàng, audit finding (internal/external), monitoring data trend xấu, hoặc yêu cầu từ cơ quan quản lý.
- Ghi nhận đầy đủ: mô tả sự cố, thời gian, địa điểm, người phát hiện, sản phẩm liên quan
- Hành động tức thời (Immediate Action): cách ly sản phẩm, dừng sản xuất nếu cần, thông báo QA
Bước 2: Đánh Giá Mức Độ Nghiêm Trọng
Phân loại CAPA theo mức độ tác động để xác định ưu tiên và timeline xử lý:
| Mức độ | Mô tả | Timeline RCA | Timeline đóng CAPA |
|---|---|---|---|
| Critical | Ảnh hưởng trực tiếp đến chất lượng sản phẩm, an toàn bệnh nhân | 5 ngày | 30 ngày |
| Major | Vi phạm GMP nghiêm trọng, có thể ảnh hưởng chất lượng sản phẩm | 10 ngày | 60 ngày |
| Minor | Vi phạm nhỏ, không ảnh hưởng trực tiếp đến sản phẩm | 15 ngày | 90 ngày |
Bước 3: Root Cause Analysis (Phân Tích Nguyên Nhân Gốc)
RCA là bước quan trọng nhất — xác định đúng nguyên nhân gốc mới có thể khắc phục triệt để. Xem chi tiết các công cụ RCA bên dưới.
Bước 4: Xác Định Hành Động Khắc Phục & Phòng Ngừa
- Corrective Action: Hành động trực tiếp lên nguyên nhân gốc đã xác định
- Preventive Action: Hành động mở rộng ra các hệ thống/quy trình tương tự để ngăn sự cố tương tự xảy ra ở nơi khác
- Mỗi hành động phải: cụ thể (Specific), đo lường được (Measurable), có người chịu trách nhiệm (Assignee), có deadline
Bước 5: Lập Kế Hoạch Thực Hiện
CAPA Plan bao gồm: danh sách hành động, người thực hiện, deadline, nguồn lực cần thiết, risk assessment cho hành động đề xuất. CAPA Plan phải được QA review và phê duyệt.
Bước 6: Triển Khai
Thực hiện các hành động theo kế hoạch, ghi nhận bằng chứng (evidence) cho mỗi hành động: SOP sửa đổi, training record, thiết bị thay thế, quy trình mới triển khai.
Bước 7: Xác Minh Hiệu Quả (Effectiveness Check)
Đây là bước nhiều tổ chức bỏ qua nhưng rất quan trọng — xem chi tiết bên dưới.
Bước 8: Đóng CAPA & Lưu Hồ Sơ
CAPA chỉ được đóng khi effectiveness check xác nhận hành động hiệu quả. QA Manager phê duyệt đóng CAPA. Toàn bộ hồ sơ lưu trữ theo GMP (tối thiểu 5 năm hoặc shelf life + 1 năm).

Công Cụ Root Cause Analysis (RCA)
5 Whys (5 Lần Hỏi Tại Sao)
Phương pháp đơn giản nhất: hỏi "Tại sao?" liên tiếp 5 lần để đi từ triệu chứng đến nguyên nhân gốc:
- Tại sao particle count phòng sạch vượt spec? → Vì HEPA filter rò rỉ
- Tại sao HEPA rò rỉ? → Vì gasket seal bị hỏng
- Tại sao gasket hỏng? → Vì không thay theo lịch bảo trì
- Tại sao không thay theo lịch? → Vì SOP bảo trì không có mục kiểm tra gasket
- Tại sao SOP thiếu? → Vì SOP chưa được review và cập nhật theo khuyến nghị nhà sản xuất
→ Nguyên nhân gốc: SOP bảo trì thiếu mục kiểm tra gasket HEPA. → CAPA: Cập nhật SOP + training + thêm checklist kiểm tra gasket.
Fishbone Diagram (Ishikawa — Sơ Đồ Xương Cá)
Phân tích theo 6M — 6 nhóm nguyên nhân tiềm ẩn:
- Man (Con người): Thiếu training, không tuân thủ SOP, mệt mỏi, rotation nhân sự
- Machine (Thiết bị): Hỏng hóc, hiệu chuẩn sai, bảo trì không đúng lịch
- Material (Nguyên vật liệu): Nguyên liệu kém chất lượng, nhà cung cấp thay đổi
- Method (Phương pháp): SOP không rõ ràng, thiếu validation, quy trình lỗi thời
- Measurement (Đo lường): Thiết bị đo sai, hiệu chuẩn hết hạn, phương pháp đo không phù hợp
- Mother Nature (Môi trường): Nhiệt độ, độ ẩm biến động, ô nhiễm ngoại lai
Fault Tree Analysis (FTA — Phân Tích Cây Lỗi)
Sơ đồ logic từ sự cố (top event) ngược về các nguyên nhân gốc. Sử dụng cổng AND/OR để mô hình hóa kết hợp nguyên nhân. Phù hợp cho sự cố phức tạp có nhiều nguyên nhân đồng thời.
CAPA Log & Tracking System
CAPA Log là sổ theo dõi trung tâm, ghi nhận tất cả CAPA trong tổ chức:
| Trường | Mô tả |
|---|---|
| CAPA ID | Mã số duy nhất (ví dụ: CAPA-2025-042) |
| Source | Nguồn: Deviation, OOS, Audit, Complaint... |
| Description | Mô tả ngắn gọn sự cố |
| Severity | Critical / Major / Minor |
| Root Cause | Nguyên nhân gốc đã xác định |
| CAPA Owner | Người chịu trách nhiệm |
| Target Date | Hạn hoàn thành |
| Status | Open / In Progress / Pending EC / Closed |
| EC Result | Effective / Not Effective |
Effectiveness Check — Đánh Giá Hiệu Quả CAPA
Effectiveness check (EC) là bước xác nhận CAPA thực sự giải quyết được vấn đề:
- Thời điểm: 30-90 ngày sau khi hoàn thành implementation (tùy mức độ)
- Phương pháp: Kiểm tra dữ liệu monitoring, deviation log, và audit observation sau CAPA
- Tiêu chí Effective: Không tái diễn cùng loại deviation trong 3-6 tháng, monitoring data trong spec, audit không phát hiện lặp lại finding
- Nếu Not Effective: Mở CAPA mới với RCA sâu hơn, xem xét nguyên nhân gốc ban đầu có đúng không
Ví Dụ CAPA Thực Tế Trong Phòng Sạch
Tình huống: Monitoring vi sinh phòng sạch Grade B phát hiện CFU vượt action limit (25 CFU thay vì <5 CFU) 2 lần liên tiếp.
- Immediate Action: Tăng tần suất vệ sinh, lấy mẫu bổ sung, kiểm tra sản phẩm liên quan
- RCA (5 Why): Vi sinh cao → do nhân viên mới chưa thạo gowning → do SOP gowning chưa đủ chi tiết → do chưa có visual SOP với hình ảnh minh họa
- CA: Tạo visual SOP gowning với hình ảnh step-by-step, re-training nhân viên mới
- PA: Áp dụng competency assessment cho gowning mỗi 6 tháng, thêm camera giám sát khu vực gowning
- EC (sau 60 ngày): Vi sinh monitoring data trở lại trong spec (<5 CFU), không tái diễn → CAPA Effective → Đóng
Cần hỗ trợ xây dựng hệ thống CAPA cho nhà máy?
Liên hệ Tư Vấn Phòng Sạch để được tư vấn thiết lập quy trình CAPA, training RCA tools, và xây dựng CAPA tracking system theo chuẩn GMP.