Tổng Quan Phòng Sạch Dược Phẩm GMP
Phòng sạch dược phẩm GMP là môi trường sản xuất được kiểm soát nghiêm ngặt về hạt bụi, vi sinh vật, nhiệt độ, độ ẩm và chênh áp — nhằm đảm bảo dược phẩm đạt tiêu chuẩn chất lượng và an toàn cho người sử dụng. Theo quy định của GMP (Good Manufacturing Practice), mọi cơ sở sản xuất thuốc đều phải có hệ thống phòng sạch phù hợp với loại sản phẩm.
Tại Việt Nam, ngành dược phẩm phải tuân thủ các tiêu chuẩn GMP do Bộ Y tế ban hành dựa trên GMP WHO và GMP EU Annex 1. Xu hướng hiện nay là nhiều nhà máy chuyển sang áp dụng GMP EU — tiêu chuẩn nghiêm ngặt hơn — để mở rộng thị trường xuất khẩu sang châu Âu, Nhật Bản và các nước CPTPP.
💡 Lưu ý chuyên gia: GMP EU Annex 1 (bản sửa đổi 2022) yêu cầu áp dụng Contamination Control Strategy (CCS) — chiến lược kiểm soát ô nhiễm toàn diện, bao gồm đánh giá rủi ro, environmental monitoring và media fill. Đây là thay đổi lớn nhất trong 20 năm qua.
Hệ Phân Loại Cấp Sạch Trong Dược Phẩm
Dược phẩm áp dụng hệ phân loại cấp A-B-C-D theo GMP, tương đương với các cấp ISO 14644. Cấp A là nghiêm ngặt nhất, đòi hỏi hệ thống HVAC với luồng khí laminar (dòng khí một chiều).

| Cấp GMP | ISO tương đương | Hạt ≥0.5µm/m³ (nghỉ) | Hạt ≥0.5µm/m³ (hoạt động) | Vi sinh CFU/m³ | Ứng dụng |
|---|---|---|---|---|---|
| A | ISO 5 | 3.520 | 3.520 | <1 | Pha chế, chiết rót vô trùng, đóng nắp vô trùng |
| B | ISO 5 (nghỉ) | 3.520 | 352.000 | 10 | Nền xung quanh vùng A trong sản xuất vô trùng |
| C | ISO 7 (nghỉ) | 352.000 | 3.520.000 | 100 | Pha chế dung dịch trước vô trùng, các bước ít quan trọng hơn |
| D | ISO 8 (nghỉ) | 3.520.000 | Không quy định | 200 | Cân, trộn, đóng gói sơ cấp sản phẩm phi vô trùng |
Sự khác biệt giữa trạng thái nghỉ và hoạt động
Trạng thái nghỉ (at rest): Phòng sạch đã hoàn tất lắp đặt, hệ thống HVAC vận hành bình thường, nhưng không có nhân viên và thiết bị hoạt động. Đây là điều kiện đo đạc sau khi xây dựng xong.
Trạng thái hoạt động (in operation): Phòng sạch đang sản xuất bình thường với đầy đủ nhân viên và thiết bị. Cấp B cho phép số hạt tăng gấp 100 lần khi hoạt động, trong khi cấp A phải duy trì nguyên trạng — đây là thách thức lớn nhất trong thiết kế.
Thiết Kế Layout Nhà Máy Dược Phẩm GMP
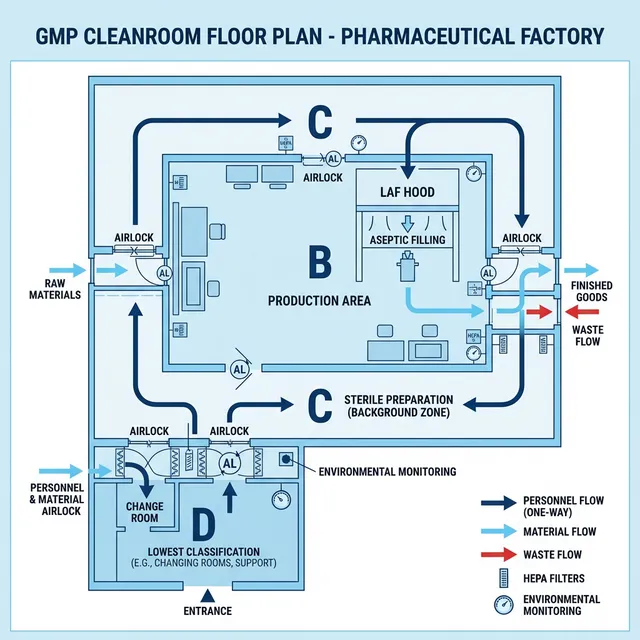
Nguyên tắc gradient áp suất
Áp suất phải giảm dần từ vùng sạch nhất ra ngoài: Cấp A → B → C → D → hành lang kỹ thuật. Chênh áp giữa các vùng liền kề tối thiểu 10-15 Pa. Hệ thống BMS (Building Management System) giám sát chênh áp 24/7, cảnh báo ngay khi có sai lệch.
Dòng chảy một chiều (One-way flow)
- Dòng nguyên liệu: Kho → cân → pha chế → chiết rót → đóng gói sơ cấp → đóng gói thứ cấp → kho thành phẩm
- Dòng nhân viên: Phòng thay đồ → tắm khí (Air Shower) → vùng sạch. Không quay lại
- Dòng rác thải: Đi riêng biệt, không giao cắt với dòng sản phẩm và nhân viên
- Dòng thiết bị: Thiết bị sau rửa → airlock → vùng sạch qua Pass Box
Airlock và phòng thay đồ
Airlock (phòng đệm): Bắt buộc giữa các vùng có cấp sạch khác nhau. Cả hai cửa không được mở đồng thời (interlocking). Airlock có cấp sạch bằng hoặc cao hơn vùng thấp hơn.
Phòng thay đồ (gowning room): Thiết kế theo kiểu cascade — mỗi bước vào vùng sạch hơn, nhân viên thay thêm một lớp đồ bảo hộ. Từ đồ thường → đồ phòng sạch cấp D → đồ cấp C → đồ vô trùng cấp B/A.
Yêu Cầu HVAC Đặc Thù Cho Dược Phẩm
So sánh chi tiết yêu cầu giữa GMP WHO và GMP EU Annex 1. Chênh áp giữa các vùng và kiểm soát vi sinh là hai yếu tố then chốt trong thiết kế hệ thống HVAC dược phẩm.
| Thông số | Cấp A-B | Cấp C | Cấp D |
|---|---|---|---|
| Kiểu luồng khí | Laminar (0.36-0.54 m/s) | Turbulent (hỗn hợp) | Turbulent |
| ACH (lần/giờ) | Laminar flow liên tục | 50-60 | 15-25 |
| Lọc cuối | HEPA H14 (≥99.995%) | HEPA H13/H14 | HEPA H13 |
| Nhiệt độ | 20-24°C (±1°C) | 20-24°C (±2°C) | 20-24°C (±2°C) |
| Độ ẩm | 45±5% RH | 45±10% RH | Kiểm soát theo sản phẩm |
| Chênh áp | +15 Pa | +10 Pa | +5 Pa |
| Recovery time | — | 15-20 phút | 15-20 phút |
Khí tươi và tuần hoàn
Phòng sạch dược phẩm thường sử dụng hệ thống AHU (Air Handling Unit) với tỷ lệ khí tươi 10-30%. Tuy nhiên, các khu vực sản xuất sản phẩm chứa penicillin, hormone, cytotoxic hoặc sinh phẩm phải sử dụng 100% khí tươi — không tuần hoàn — để tránh chéo nhiễm.
Thiết Bị Chuyên Dụng Trong Phòng Sạch Dược Phẩm
LAF (Laminar Air Flow)
Tủ cấp khí laminar tạo vùng cấp A cho các thao tác vô trùng mở (open processing). Luồng khí HEPA đi từ trên xuống hoặc từ sau ra trước với vận tốc 0.36-0.54 m/s. LAF phù hợp cho các thao tác đơn giản: pha chế thủ công, kiểm nghiệm, lấy mẫu.
Isolator
Hệ thống kín hoàn toàn, tách biệt sản phẩm với môi trường và người vận hành. Thao tác qua găng tay (glove port) hoặc tay áo (half-suit). Isolator được khử trùng bằng VHP (Vaporized Hydrogen Peroxide) trước mỗi mẻ sản xuất. GMP EU Annex 1 (2022) khuyến khích sử dụng isolator thay thế LAF truyền thống.
RABS (Restricted Access Barrier System)
Hệ trung gian giữa LAF và isolator — có rào cản vật lý (cửa kính, tấm chắn) nhưng không kín hoàn toàn. RABS chia thành hai loại:
- Passive RABS (mở): Có cửa mở để can thiệp, đặt trong background cấp B
- Active RABS (đóng): Cửa chỉ mở khi cần thiết, hệ thống cấp khí riêng
Quy Trình Vệ Sinh & Khử Trùng
Vệ sinh phòng sạch dược phẩm phải tuân theo SOP (Standard Operating Procedure) được thẩm định:
- Vệ sinh hàng ngày: Lau sàn, tường, bề mặt thiết bị bằng chất tẩy rửa đã được phê duyệt
- Khử trùng hàng tuần: Sử dụng hóa chất khử trùng (IPA 70%, sodium hypochlorite, peracetic acid)
- Xông phòng định kỳ: VHP (Vaporized Hydrogen Peroxide) hoặc formaldehyde cho toàn bộ phòng
- Luân chuyển hóa chất: Thay đổi loại hóa chất khử trùng theo chu kỳ để tránh vi sinh vật kháng thuốc
💡 Lưu ý chuyên gia: GMP EU Annex 1 yêu cầu chương trình khử trùng phải bao gồm sporicidal agent (tác nhân diệt bào tử) được sử dụng theo tần suất xác định. Việc chỉ dùng IPA 70% là không đủ — cần bổ sung chất diệt bào tử như peracetic acid.
Environmental Monitoring (EM) — Giám Sát Môi Trường
Environmental monitoring là chương trình giám sát liên tục các điều kiện môi trường sản xuất, bao gồm:
Giám sát hạt (Particle Monitoring)
- Cấp A-B: Giám sát liên tục (continuous monitoring) bằng particle counter online
- Cấp C-D: Giám sát theo tần suất quy định (periodic monitoring)
- Đo hạt ≥0.5µm và ≥5.0µm tại các vị trí đã thẩm định
Giám sát vi sinh (Microbiological Monitoring)
- Air sampling (lấy mẫu khí): Active air sampler (SAS, MAS) — hút lượng khí xác định qua đĩa thạch
- Settle plates (đĩa lắng): Đĩa thạch phơi trong 4 giờ (cấp A-B) hoặc theo SOP
- Contact plates (đĩa tiếp xúc): Lấy mẫu bề mặt thiết bị, sàn, tường
- Glove print: In dấu găng tay lên đĩa thạch — kiểm tra vệ sinh tay nhân viên
Media Fill Test
Media fill (Process Simulation Test) là thử nghiệm bắt buộc cho dây chuyền sản xuất vô trùng. Toàn bộ quy trình được mô phỏng bằng môi trường nuôi cấy (TSB - Tryptic Soy Broth) thay cho sản phẩm thực. Sau đó ủ ấm 14 ngày ở hai nhiệt độ (20-25°C và 30-35°C). Nếu có mẫu nào đục (vi sinh vật phát triển), quy trình bị đánh giá là không đạt.
Chi Phí Tham Khảo Xây Phòng Sạch Dược Phẩm
| Cấp sạch | Chi phí/m² (VNĐ) | Bao gồm | Ghi chú |
|---|---|---|---|
| Cấp D (ISO 8) | 3 - 5 triệu | Vách panel, trần, sàn, HVAC cơ bản | Phù hợp đóng gói, kho |
| Cấp C (ISO 7) | 5 - 8 triệu | HVAC tiên tiến, HEPA H14 | Pha chế phi vô trùng |
| Cấp B (ISO 5 nghỉ) | 8 - 12 triệu | AHU riêng, EM online | Background cho cấp A |
| Cấp A (LAF/Isolator) | 15 - 25 triệu | LAF/Isolator, particle counter | Chiết rót vô trùng |
Chi phí trên chưa bao gồm: hệ thống nước tinh khiết (PW/WFI), hệ thống khí nén sạch, BMS, thẩm định IQ/OQ/PQ. Tổng chi phí dự án thực tế thường gấp 1.5-2 lần chi phí xây phòng sạch đơn thuần.
Sai Lầm Thường Gặp Khi Xây Phòng Sạch Dược Phẩm
- Thiết kế không đủ chênh áp: Nhiều dự án chỉ tính chênh áp khi cửa đóng, quên rằng khi mở cửa (airlock) chênh áp sẽ giảm. Cần tính toán lưu lượng bù đủ cho cả hai trạng thái.
- Không dự phòng environmental monitoring: Lắp đặt hệ thống mà không quy hoạch vị trí đặt particle counter và air sampler ngay từ đầu. Việc bổ sung sau sẽ tốn kém và phải thẩm định lại.
- Bỏ qua recovery time test: Phòng sạch phải đạt cấp sạch yêu cầu trong vòng 15-20 phút sau khi kết thúc hoạt động (clean-up period). Nếu không đạt, cần tăng ACH hoặc điều chỉnh luồng khí.
- Layout chéo dòng chảy: Dòng nguyên liệu, sản phẩm, nhân viên và rác thải giao nhau → nguy cơ chéo nhiễm (cross-contamination) rất cao.
- Không luân chuyển hóa chất khử trùng: Dùng mãi một loại hóa chất → vi sinh vật phát triển khả năng kháng → kết quả EM xấu dần.
💡 Lưu ý chuyên gia: Trước khi xây phòng sạch dược phẩm, hãy lập Contamination Control Strategy (CCS) theo GMP EU Annex 1. CCS giúp xác định rủi ro ô nhiễm tại từng công đoạn và thiết kế biện pháp kiểm soát phù hợp — tránh lãng phí đầu tư vào những khu vực không cần thiết.
Bạn cần tư vấn thiết kế phòng sạch dược phẩm GMP?
Liên hệ đội ngũ chuyên gia của chúng tôi để được hỗ trợ miễn phí — từ khảo sát, thiết kế layout, đến lựa chọn thiết bị HVAC và lập kế hoạch thẩm định.
📞 Nhận tư vấn miễn phí ngay →