Lịch Sử Phát Triển GMP WHO
GMP (Good Manufacturing Practice) của WHO ra đời để đảm bảo dược phẩm đạt chất lượng trên toàn cầu, đặc biệt tại các nước đang phát triển. Quá trình phát triển kéo dài hơn 50 năm:
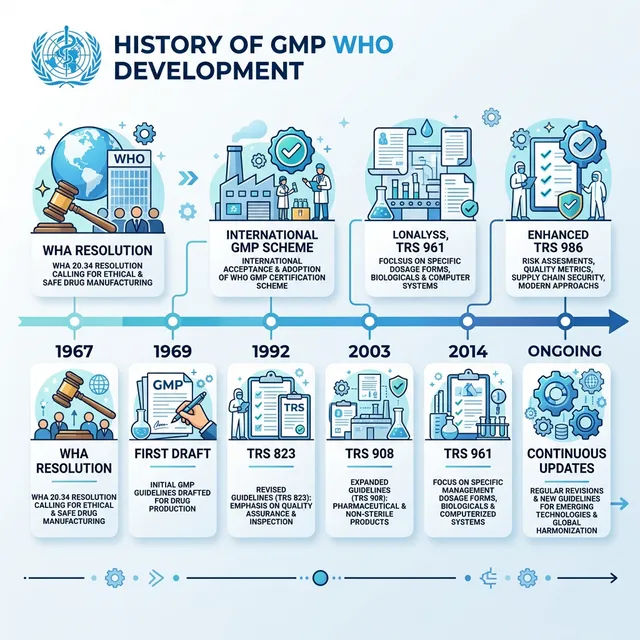
- 1967: Nghị quyết WHA 20.34 — Đại hội đồng Y tế Thế giới yêu cầu WHO xây dựng hướng dẫn GMP
- 1969: Phiên bản đầu tiên "Good Practices in the Manufacture and Quality Control of Drugs"
- 1975: WHO Certification Scheme — hệ thống chứng nhận GMP giữa các nước thành viên
- 1992: TRS 823 — cập nhật lớn, bổ sung yêu cầu validation và documentation
- 2003: TRS 908 Phụ lục 4 — nâng cấp yêu cầu về phòng sạch, thiết bị
- 2011: TRS 961 — bổ sung Phụ lục 5 (HVAC), Phụ lục 6 (nước dược phẩm)
- 2014: TRS 986 Phụ lục 2 — phiên bản hiện hành, cập nhật toàn diện về phòng sạch và sản xuất vô trùng
Cấu Trúc Tài Liệu TRS 986
TRS 986 (2014) là tài liệu tham chiếu chính cho GMP WHO hiện hành. Các phụ lục quan trọng nhất cho phòng sạch:
| Phụ lục | Nội dung | Áp dụng cho |
|---|---|---|
| TRS 986, Phụ lục 2 | GMP tổng quát — phòng xưởng, thiết bị, nhân sự, validation | Tất cả nhà máy dược |
| TRS 961, Phụ lục 5 | Hệ thống HVAC — thiết kế, vận hành, qualification | Phòng sạch dược phẩm |
| TRS 957, Phụ lục 4 | Nước dược phẩm — PW, WFI, hệ thống loop | Hệ thống nước |
| TRS 937, Phụ lục 6 | Validation — IQ, OQ, PQ, process validation | Qualification & validation |
| TRS 961, Phụ lục 6 | Sản xuất sản phẩm vô trùng — phòng sạch A-D | Nhà máy vô trùng |
Phân Loại Cấp Sạch A-B-C-D
GMP WHO phân loại phòng sạch dược phẩm theo 4 cấp, tương tự GMP EU Annex 1 nhưng linh hoạt hơn:
| Cấp | ISO (nghỉ) | Hạt ≥0.5µm/m³ (nghỉ) | Hạt ≥0.5µm/m³ (HĐ) | Hạt ≥5.0µm/m³ (nghỉ) | Ứng dụng |
|---|---|---|---|---|---|
| A | ISO 5 | 3.520 | 3.520 | 20 | Chiết rót vô trùng, pha chế |
| B | ISO 5 | 3.520 | 352.000 | 29 | Nền xung quanh vùng A |
| C | ISO 7 | 352.000 | 3.520.000 | 2.900 | Pha chế thuốc uống, bào chế |
| D | ISO 8 | 3.520.000 | Không quy định | 29.000 | Cân, trộn, đóng gói sơ |
Yêu Cầu Vi Sinh Theo GMP WHO
| Cấp | Mẫu khí (CFU/m³) | Đĩa lắng 90mm (CFU/4h) | Tiếp xúc (CFU/plate) | Găng tay (CFU/5 ngón) |
|---|---|---|---|---|
| A | <1 | <1 | <1 | <1 |
| B | 10 | 5 | 5 | 5 |
| C | 100 | 50 | 25 | — |
| D | 200 | 100 | 50 | — |
Yêu Cầu HVAC Theo WHO TRS 961 Phụ Lục 5
TRS 961 Phụ lục 5 là hướng dẫn chi tiết nhất của WHO về hệ thống HVAC phòng sạch dược phẩm:
- Nhiệt độ: 20-24°C cho sản xuất, ±2°C cho khu vực critical
- Độ ẩm: 45-55% RH cho sản xuất chung, ≤35% cho effervescent
- Chênh áp: Tối thiểu 10 Pa giữa các vùng khác cấp sạch, 15 Pa giữa phòng sạch và bên ngoài
- ACH: Cấp A (laminar 0.36-0.54 m/s), Cấp B (50-60 ACH), Cấp C (25-40 ACH), Cấp D (15-25 ACH)
- Lọc: HEPA H14 cho cấp A-B, HEPA H13 cho cấp C-D
- Recovery time: ≤15-20 phút cho cấp B-C
So Sánh Chi Tiết: GMP WHO vs GMP EU

| Tiêu chí | GMP WHO | GMP EU (Annex 1) |
|---|---|---|
| Phạm vi áp dụng | Toàn cầu, >100 nước | EU, PIC/S (~55 nước) |
| Mức độ nghiêm ngặt | Linh hoạt, phù hợp nước đang phát triển | Nghiêm ngặt nhất thế giới |
| CCS bắt buộc? | Không yêu cầu chính thức | Bắt buộc (2023) |
| RABS/Isolator | Không yêu cầu cụ thể | Khuyến nghị mạnh |
| EM liên tục cấp A | Khuyến nghị | Bắt buộc liên tục |
| Data Integrity | Đề cập chung | Yêu cầu chi tiết ALCOA+ |
| Giám sát hạt ≥5µm cấp A | Khuyến nghị | Bắt buộc real-time |
| Phiên bản mới nhất | TRS 986 (2014) | Annex 1 (2022/2023) |
Áp Dụng GMP WHO Tại Việt Nam
Việt Nam áp dụng GMP WHO làm tiêu chuẩn bắt buộc cho ngành dược phẩm:
- Thông tư 35/2018/TT-BYT: Quy định GMP WHO là tiêu chuẩn tối thiểu cho nhà máy sản xuất thuốc
- Cục Quản lý Dược (DAV): Cơ quan cấp giấy chứng nhận GMP, thanh tra định kỳ 3 năm
- Lộ trình PIC/S: Việt Nam nộp đơn gia nhập PIC/S từ 2018, đang hài hòa hóa tiêu chuẩn → dần tiến đến mức EU GMP
- Nhà máy xuất khẩu: Nếu xuất EU → phải đạt EU GMP. Xuất Nhật → PIC/S GMP. Xuất Mỹ → cGMP FDA
- Số lượng: Tính đến 2024, Việt Nam có hơn 250 nhà máy đạt GMP WHO, ~15 nhà máy đạt EU GMP/PIC/S
Quy Trình Đạt Chứng Nhận GMP WHO Tại Việt Nam
- Xây dựng nhà xưởng: Thiết kế, thi công phòng sạch theo GMP layout
- Qualification: IQ/OQ/PQ cho HVAC, nước, thiết bị
- Xây dựng hồ sơ: SOP, validation protocol, training record, EM program
- Tự thanh tra: Internal audit theo checklist GMP WHO
- Nộp hồ sơ DAV: Đơn đăng ký + hồ sơ nhà máy
- Thanh tra DAV: Đoàn thanh tra thực địa 3-5 ngày
- Khắc phục: Trả lời observation, thực hiện CAPA
- Cấp chứng nhận: GMP WHO có hiệu lực 3 năm
💡 Lưu ý chuyên gia: GMP WHO đang dần "hội tụ" với EU GMP khi Việt Nam tiến trình gia nhập PIC/S. Nhà máy xây mới nên thiết kế theo tiêu chuẩn EU GMP/PIC/S ngay từ đầu — tránh phải nâng cấp tốn kém sau này. Chi phí xây theo PIC/S chỉ đắt hơn 10-15% so với WHO, nhưng giá trị chứng nhận quốc tế cao hơn nhiều.
Bạn cần tư vấn xây dựng nhà máy đạt GMP WHO?
📞 Nhận tư vấn miễn phí ngay →