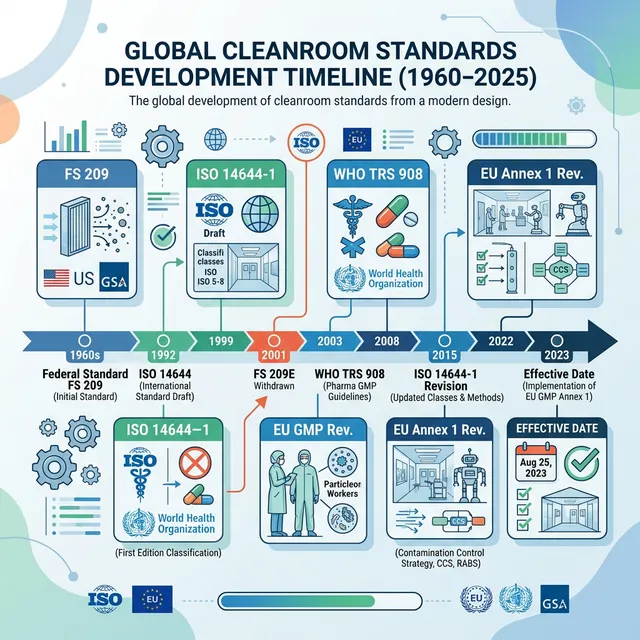
Timeline Phát Triển Các Tiêu Chuẩn Phòng Sạch
| Năm | Sự kiện | Ý nghĩa |
|---|---|---|
| 1963 | FS 209 (US Federal Standard) | Tiêu chuẩn phòng sạch đầu tiên — phân loại Class 1 đến Class 100,000 |
| 1967 | WHO WHA 20.34 | Nghị quyết xây dựng GMP cho dược phẩm |
| 1992 | ISO/TC 209 thành lập | Bắt đầu xây dựng tiêu chuẩn ISO 14644 quốc tế |
| 1999 | ISO 14644-1:1999 | Tiêu chuẩn phòng sạch quốc tế đầu tiên — ISO 1-9 |
| 2001 | FS 209E bãi bỏ | Mỹ chấp nhận ISO 14644 thay thế FS 209 |
| 2008 | EU GMP Annex 1 revision | Cập nhật yêu cầu sản xuất vô trùng |
| 2011 | TCVN 8664:2011 | Việt Nam chấp nhận ISO 14644 |
| 2014 | WHO TRS 986 | Phiên bản GMP WHO hiện hành |
| 2015 | ISO 14644-1:2015 | Cập nhật lớn — bỏ bảng U, thêm macro test |
| 2022/2023 | EU Annex 1 mới | Thay đổi lớn nhất 14 năm — CCS bắt buộc |
Bảng Tổng Hợp So Sánh Các Tiêu Chuẩn
Bảng so sánh giữa ISO 14644, GMP WHO, GMP EU Annex 1, cGMP FDA và TCVN 8664:
| Tiêu chí | ISO 14644 | GMP EU | GMP WHO | cGMP FDA | FS 209E | TCVN 8664 |
|---|---|---|---|---|---|---|
| Phạm vi | Toàn cầu | EU/PIC-S | Toàn cầu | Mỹ | Đã bãi bỏ | Việt Nam |
| Hệ phân loại | ISO 1-9 | A-B-C-D | A-B-C-D | Không chính thức | Class 1-100K | ISO 1-9 |
| Đơn vị đo | Hạt/m³ | Hạt/m³ + CFU | Hạt/m³ + CFU | Hạt/ft³ hoặc m³ | Hạt/ft³ | Hạt/m³ |
| Vi sinh | Không bắt buộc | Bắt buộc | Bắt buộc | Không cụ thể | Không | Không bắt buộc |
| Trạng thái đo | As-built, At-rest, In-operation | Nghỉ & HĐ | Nghỉ & HĐ | Hoạt động | Hoạt động | 3 trạng thái |
| Phiên bản mới nhất | 2015/2019 | 2023 | 2014 | Liên tục | Bãi bỏ 2001 | 2011 |
| Mức độ nghiêm ngặt | Trung bình | Rất cao | Trung bình | Cao | — | = ISO |
So Sánh Chi Tiết Theo Tiêu Chí
Hạt bụi & ACH
- ISO 14644: Quy định giới hạn hạt, KHÔNG quy định ACH — để nhà thiết kế tự chọn
- GMP EU/WHO: Quy định giới hạn hạt VÀ vi sinh. ACH khuyến nghị nhưng không bắt buộc cụ thể
- FS 209E: Dùng hạt/ft³ — Class 100 = 100 hạt ≥0.5µm/ft³ ≈ ISO 5
Chênh áp
- ISO 14644-4: Khuyến nghị 5-20 Pa (linh hoạt)
- GMP EU Annex 1: Tối thiểu 10 Pa giữa các cấp, khuyến nghị 10-15 Pa
- GMP WHO TRS 961: Tối thiểu 10-15 Pa giữa các cấp
- cGMP FDA: "Positive pressure differential" — không quy định số cụ thể
Vi sinh
- ISO 14644: KHÔNG quy định vi sinh — chỉ hạt bụi
- GMP EU: Quy định chi tiết CFU/m³, đĩa lắng, tiếp xúc, găng tay — cho cả 4 cấp A-D
- GMP WHO: Giống EU nhưng linh hoạt hơn về tần suất monitoring
- cGMP FDA: Yêu cầu EM nhưng không quy định giới hạn cụ thể trong regulation — chỉ trong guidance
Bảng Quy Đổi Cấp Sạch
| ISO 14644 | GMP EU/WHO | FS 209E | TCVN 8664 | Ứng dụng |
|---|---|---|---|---|
| ISO 3 | — | Class 1 | TCVN 8664-1 Cấp 3 | Fab bán dẫn |
| ISO 4 | — | Class 10 | Cấp 4 | Điện tử, nano |
| ISO 5 | A / B (at-rest) | Class 100 | Cấp 5 | Vô trùng, chiết rót |
| ISO 6 | — | Class 1,000 | Cấp 6 | Lắp ráp điện tử |
| ISO 7 | C (at-rest) | Class 10,000 | Cấp 7 | Sản xuất dược phẩm |
| ISO 8 | D (at-rest) | Class 100,000 | Cấp 8 | Đóng gói, kho |
Ma Trận: Ngành × Tiêu Chuẩn Áp Dụng

| Ngành | Tiêu chuẩn chính | Tiêu chuẩn bổ sung | Cấp sạch phổ biến |
|---|---|---|---|
| Dược phẩm (nội địa VN) | GMP WHO | TCVN 8664, ISO 14644 | C-D (ISO 7-8) |
| Dược phẩm (xuất khẩu EU) | GMP EU/PIC-S | ISO 14644 | A-B-C-D (ISO 5-8) |
| Dược phẩm (xuất khẩu Mỹ) | cGMP FDA | USP <797>, <800> | ISO 5-8 |
| Điện tử/Bán dẫn | ISO 14644 | SEMI S2, IEST | ISO 1-5 |
| Thiết bị y tế | ISO 14644 + ISO 13485 | FDA 21 CFR 820, EU MDR | ISO 7-8 |
| Thực phẩm | ISO 14644 + HACCP | ISO 22000, FSSC 22000 | ISO 7-8 |
| Mỹ phẩm | CGMP ASEAN | ISO 22716, ISO 14644 | ISO 7-8 |
| Bệnh viện | ASHRAE 170 | TCVN, FGI Guidelines | ISO 5-7 (phòng mổ) |
Cách Chọn Tiêu Chuẩn Phù Hợp Cho Dự Án
- Xác định ngành: Dược phẩm, điện tử, thực phẩm, y tế, mỹ phẩm?
- Xác định thị trường: Nội địa VN, xuất EU, xuất Mỹ, ASEAN?
- Tra ma trận: Dùng bảng ngành × tiêu chuẩn ở trên
- Xác định cấp sạch: Dùng bảng quy đổi → chọn ISO class phù hợp
- Thiết kế theo tiêu chuẩn cao nhất: Nếu xuất nhiều thị trường, thiết kế theo tiêu chuẩn nghiêm ngặt nhất (EU GMP) → tự động đạt các tiêu chuẩn thấp hơn
Xu Hướng Tương Lai Tiêu Chuẩn Phòng Sạch
- Hội tụ quốc tế: PIC/S đang hài hòa hóa GMP toàn cầu — WHO, EU, FDA dần tiến đến một chuẩn chung
- Giám sát real-time: Từ lấy mẫu định kỳ → continuous monitoring (hạt, vi sinh rapid methods)
- Risk-based approach: Tiêu chuẩn mới tập trung vào đánh giá rủi ro (CCS) thay vì checklist cứng nhắc
- Barrier systems: RABS/Isolator sẽ thay thế dần phòng sạch truyền thống cho sản xuất vô trùng
- Digitalization: e-QMS, paperless GMP, AI-assisted EM trending
💡 Lưu ý chuyên gia: Đừng chọn tiêu chuẩn "vừa đủ" — hãy thiết kế theo tiêu chuẩn cao hơn nhu cầu hiện tại 1 bậc. Chi phí xây theo PIC/S chỉ đắt hơn 10-15% so với WHO GMP, nhưng mở ra cơ hội xuất khẩu toàn cầu. Xây dựng phòng sạch là đầu tư 20-30 năm — tiêu chuẩn chỉ ngày càng nghiêm ngặt hơn.
Bạn cần tư vấn chọn tiêu chuẩn và thiết kế phòng sạch phù hợp?
📞 Nhận tư vấn miễn phí ngay →
Câu Hỏi Thường Gặp (FAQ)
FS 209E đã bãi bỏ sao vẫn thấy dùng?
FS 209E bãi bỏ 2001, nhưng cách gọi "Class 100, Class 10,000" vẫn phổ biến trong giao tiếp vì dễ nhớ. Tài liệu chính thức nên dùng ISO 14644.
Nhà máy dược cần áp dụng ISO 14644 hay GMP?
Cần CẢ HAI. ISO 14644 để phân loại và kiểm tra phòng sạch. GMP (WHO/EU) để quy định cấp sạch tại mỗi khu vực sản xuất, yêu cầu vi sinh, và quản lý chất lượng.
Tiêu chuẩn nào mới nhất, toàn diện nhất?
GMP EU Annex 1 (2023) cho dược phẩm vô trùng — nghiêm ngặt nhất. ISO 14644-1:2015 cho phân loại phòng sạch chung. TCVN 8664:2011 cho pháp lý Việt Nam (nhưng đang lỗi thời).
Nhà máy Việt Nam xuất khẩu nên theo tiêu chuẩn nào?
Xuất EU → EU GMP/PIC/S. Xuất Mỹ → cGMP FDA. Xuất Nhật, Úc, Canada → PIC/S. Xuất ASEAN → GMP WHO + ACTD. Nội địa → GMP WHO (tối thiểu) + TCVN 8664.