Tổng Quan Về GLP (Good Laboratory Practice)
GLP là hệ thống chất lượng cho phòng thí nghiệm thực hiện nghiên cứu phi lâm sàng (non-clinical) về an toàn sức khỏe và môi trường. GLP đảm bảo dữ liệu nghiên cứu là đáng tin cậy, có thể tái tạo, và tuân thủ đạo đức khoa học.
GLP áp dụng cho: nghiên cứu độc tính dược phẩm, thử nghiệm an toàn hóa chất, thử nghiệm thuốc bảo vệ thực vật, nghiên cứu phụ gia thực phẩm, và sản phẩm công nghiệp mới.
OECD GLP Principles — Các Nguyên Tắc Cốt Lõi
OECD ban hành GLP Principles (ENV/MC/CHEM(98)17) gồm các phần chính:
- Tổ chức và nhân sự: Trách nhiệm Management, Study Director, QAU (Quality Assurance Unit), nhân viên kỹ thuật
- Chương trình đảm bảo chất lượng: QAU độc lập — thanh tra study, kiểm tra SOP compliance, báo cáo management
- Cơ sở vật chất: Phòng lab, phòng nuôi động vật, kho mẫu, kho hóa chất — phải tách biệt phù hợp
- Thiết bị, vật liệu, thuốc thử: Hiệu chuẩn, bảo trì, kiểm tra chất lượng thuốc thử
- Hệ thống thử nghiệm: Động vật thí nghiệm, nuôi cấy tế bào, mẫu sinh học — tiêu chuẩn chăm sóc
- Test items và reference items: Nhận dạng, bảo quản, xử lý chất thử nghiệm
- SOPs (Quy trình thao tác chuẩn): Mọi hoạt động phải có SOP, được phê duyệt và phổ biến
- Thực hiện study: Study plan, tiến hành, ghi chép, thay đổi phải documented
- Báo cáo kết quả: Final report bởi Study Director, QA statement
- Lưu trữ hồ sơ và mẫu: Archive theo quy định — tối thiểu 15 năm hoặc suốt vòng đời sản phẩm
Yêu Cầu Phòng Thí Nghiệm GLP

- Phân tách rõ ràng: Phòng hóa học, vi sinh, nuôi cấy tế bào, phòng động vật, kho mẫu, kho hóa chất — tách biệt vật lý hoặc quản lý
- Phòng sạch vi sinh: ISO 7-8, có laminar flow hood hoặc BSC Class II
- Kiểm soát môi trường: Nhiệt độ 20-25°C (±2°C), độ ẩm 45-65% RH, âm thanh <65 dB(A)
- Hệ thống nước: Type I (ultrapure, <0.1 µS/cm), Type II (≤1 µS/cm), Type III (≤5 µS/cm) theo ASTM
- Thiết bị phân tích: HPLC, GC, UV-Vis, Karl Fischer — calibrated và qualified (IQ/OQ)
- Quản lý chất thải: Phân loại (hóa chất, sinh học, phóng xạ), xử lý theo QCVN
- Archive room: Chống cháy, chống ẩm, kiểm soát truy cập, nhiệt độ/ẩm ổn định
BSL Levels (Biosafety Levels) — Phân Cấp An Toàn Sinh Học
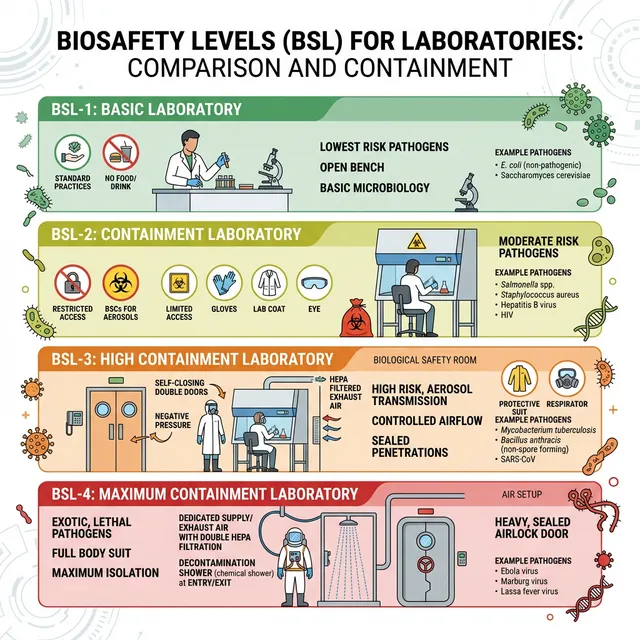
| Cấp | Mầm bệnh | Phòng sạch | Thiết bị an toàn | Ví dụ |
|---|---|---|---|---|
| BSL-1 | Không gây bệnh cho người | Không yêu cầu | Bàn thí nghiệm mở | E.coli K12, Bacillus subtilis |
| BSL-2 | Gây bệnh nhẹ-trung bình | Khuyến nghị | BSC Class II, autoclave | Staph. aureus, Salmonella, HIV |
| BSL-3 | Gây bệnh nặng, có vaccine/thuốc | ISO 7-8, áp suất âm | BSC III, HEPA, áp âm | TB, SARS-CoV-2, Brucella |
| BSL-4 | Gây bệnh chết, không có thuốc | Kín hoàn toàn | Bộ đồ áp suất dương, chemical shower | Ebola, Marburg, Nipah |
BSL-3 và BSL-4 yêu cầu HVAC đặc biệt: áp suất âm, lọc HEPA khí thải, không tuần hoàn khí, airlock vào/ra với khử trùng.
Data Integrity — Tính Toàn Vẹn Dữ Liệu
Data integrity là yêu cầu then chốt của GLP — dữ liệu nghiên cứu phải tuân thủ nguyên tắc ALCOA+:
- Attributable — Có thể gán cho người thực hiện
- Legible — Đọc được, rõ ràng, lâu bền
- Contemporaneous — Ghi nhận tại thời điểm thực hiện
- Original — Dữ liệu gốc (raw data), không sao chép
- Accurate — Chính xác, không chỉnh sửa trái phép
- +Complete, Consistent, Enduring, Available
Hệ thống quản lý dữ liệu: LIMS (Laboratory Information Management System), Chromatography Data System (CDS) — phải có audit trail, electronic signature, backup.
GLP vs GMP vs ISO 17025
| Tiêu chí | GLP | GMP (Phần QC) | ISO 17025 |
|---|---|---|---|
| Áp dụng cho | Nghiên cứu an toàn phi lâm sàng | Kiểm tra chất lượng sản phẩm | Phòng thử nghiệm/hiệu chuẩn |
| Mục đích | Dữ liệu đáng tin cậy | Sản phẩm đạt chất lượng | Năng lực kỹ thuật phòng lab |
| Cơ quan quản lý | OECD, WHO | FDA, EMA, Bộ Y tế | ISO, ILAC, BOA |
| Study Director | Bắt buộc (1 per study) | Không yêu cầu | Không yêu cầu |
| QA Unit độc lập | Bắt buộc | Không bắt buộc riêng | Không yêu cầu |
| Archive | ≥15 năm | ≥5 năm | Theo chính sách |
| Phòng sạch | BSL + ISO 7-8 (vi sinh) | ISO 5-8 (tùy sản phẩm) | Theo nhu cầu |
GLP Tại Việt Nam
- Bộ KH&CN: Cấp chứng nhận GLP cho phòng thí nghiệm an toàn
- Bộ Y tế / Cục QLD: Giám sát phòng kiểm nghiệm thuốc theo GMP Phần 2
- Số lượng: Việt Nam có ~30 phòng thí nghiệm đạt GLP/GMP QC chính thức
- Xu hướng: Tăng cường năng lực BSL-3 sau COVID-19, đầu tư phòng bioequivalence cho generic drug
💡 Lưu ý chuyên gia: Phòng thí nghiệm dược phẩm ở Việt Nam thường cần đạt ĐỒNG THỜI GMP phần QC (cho kiểm tra sản phẩm) và GLP (nếu có nghiên cứu an toàn). Hai hệ thống bổ trợ nhau — GLP tập trung vào quy trình nghiên cứu, GMP tập trung vào kiểm soát chất lượng sản phẩm.
Bạn cần tư vấn thiết kế phòng thí nghiệm GLP?
📞 Nhận tư vấn miễn phí ngay →